국내 신생 자돈에서 발생한 선천성 돈두 증례보고
Congenital swinepox of neonatal pigs in a Korean domestic farm
Article information
Trans Abstract
Three neonatal pigs from the same litter in a domestic farm were born with skin lesions. Grossly, multiple well-circumscribed, round papules distributed over the skin of the three piglets. Two piglets were submitted for a diagnosis of skin disease. Microscopically, epidermal hyperplasia with ballooning degeneration of stratum spinosum keratinocytes was observed. Some keratinocytes contained eosinophilic intracytoplasmic inclusions and a central nuclear vacuole and chromatin margination. Swinepox (SWP) virus was detected by polymerase chain reaction and nucleotide sequencing, and Staphylococcus hyicus was isolated in skin lesions. Based on the gross findings and laboratory results, these piglets were diagnosed with congenital SWP with a secondary staphylococcal infection.
돈두(豚痘, swinepox, SWP)는 돼지에서만 발생하는 급성의 바이러스성 피부 질병으로 남북미[1-4], 유럽[5], 아시아[6,7] 등 전세계적인 발생 분포를 보인다[8]. 원인체인 돈두바이러스(swinepox virus, SWPV)는 Poxviridae, Suipoxvirus속이며, 외피(envelope)로 둘러싸여 있고 이중 가닥의 D NA를 가진 벽돌 모양(brick-shaped)의 대형 바이러스이다[8,9]. 3-4개월령의 어린 자돈에서는 이환율이 100%에 이르기도 하고 심한 증상을 나타내는 반면, 성돈에서는 경미한 병변을 유발하고 시간이 경과함에 따라 자가 치유되는 경향을 보인다[3,8-10]. 일반적으로 SWPV의 전파는 바이러스에 오염된 물질이 손상된 피부에 직접 또는 간접적으로 접촉하여 발생한다[9]. 또한 SWPV는 돼지 이(Haematopinus suis)에 의한 기계적 전파가 가능하며[8,9], 드물게 선천적 감염 사례도 보고되고 있다[2,4,8]. 본 증례는 국내 양돈 농장에서 발생한 신생 자돈의 SWP 발병 예로 이에 대한 특징적인 육안 및 병리조직학적 소견과 미생물학적 검사 결과를 정리하여 보고하고자 한다.
2018년 5월, 전남 나주시 소재 모돈 400두 규모의 자돈생산농장(farrow-to-nursery farm)에 사육중인 3산차 모돈으로부터 태어난 13두의 신생 자돈 중 4두에서 비정상적인 피부 병변이 관찰되었다. 3두는 활력이 현저하게 저하되고 전신에 원형의 융기되고 가피가 덮인 구진(papule)성 병변이 산재해 있었다. 나머지 1두는 양쪽 대퇴부 피부의 일부가 완전 결손되어 진피층이 노출되어 있었으며, 불완전상피발생(epitheliogenesis imperfecta)으로 진단되었다. 피부 병변이 관찰된 3두의 신생 자돈 중에서 2두에 대하여 확진을 위한 부검을 실시하였다. 육안적으로 피부와 내부 장기의 이상 여부를 확인한 뒤, 병리조직학적 검사를 위하여 피부 조직을 포함하여 채취한 장기는 10% 중성 완충포르말린 용액에 고정하였다. 고정이 완료된 조직은 일반적인 조직처리 방법에 준하여 파라핀 포매 후 hematoxylin & eosin 염색을 실시하였으며, 추가 피부 절편에 대하여 Gram 염색을 진행하였다. SWPV 감염 여부를 확인하기 위하여 피부 유제로부터 D NA를 추출하여 중합효소연쇄반응(polymerase chain reaction, PCR)을 실시하였다. Primer는 기존에 보고된 viral late transcription factor-3 (VLTF-3) 유전자 부위를 증폭하는 VLTF: 5’-TAGTTTCAGAACAAGGATATG-3’ 및 VLTR: 5’-TCCCA TATTAATTGATTACT-3’를 사용하였다[1,6]. PCR 반응 조건은 94°C에 5분간 반응시킨 다음, 94°C 30초, 49°C 30초 및 72°C 45초씩 30회 반복하고 최종 72°C에서 10분간 반응하였다[6]. PCR 산물은 1.5% agarose gel 상에서 전기 영동을 실시하였고 SWPV 특이적인 524 bp의 밴드 유무를 확인하였다. 또한 세균성 병원체의 감별을 위하여 피부 병변 부위에서 세균배양검사를 진행하였다. PCR 양성 결과물에 대한 염기서열분석은 마크로젠(Korea)에 의뢰하였다. 상기 염기서열에 대한 계통학적 유연관계 분석은 MEGA7 program (http://www.megasoftware.net)을 사용하였으며, 미국 국립생물공학정보센터(National Center for Biotechnology Information, NCBI)의 GeneBank에 등록된 8종의 poxvirus VLTF-3 유전자 염기서열과 비교 분석하였다.
부검 결과, 신생 자돈의 피부에는 직경 약 5 mm 내외 자적색 또는 적색의 원형 또는 난원형으로 융기된 구진 또는 농포(pustule)가 두부, 귀, 목, 등, 배, 사지 등 전신에 걸쳐 분포하고 있었다(Fig. 1). 내부 장기에서는 신장 수질부의 황갈색 요산염(urate) 침착 이외에 특별한 육안적 변화를 관찰할 수 없었다. 병리조직학적으로 피부의 표피층은 다병소성으로 중등도 내지 심하게 상피세포가 증식하여 현저하게 비후되어 있었으며, 주로 가시층(stratum spinosum) 내 각질세포(keratinocyte)의 풍선변성(ballooning degeneration)이 두드러지게 관찰되었다(Fig. 2). 일부 병변의 중심부는 국소적으로 괴사되어 궤양을 형성하거나 손상된 표피층 위에 괴사된 세포붕괴물과 염증세포로 구성된 가피가 부착되어 있었다. 변성된 각질세포의 핵은 크고 중심에 공포를 형성하여 투명하게 관찰되었고 비정상적으로 종창된 세포질 내에는 호산성 봉입체(eosinophilic inclusion body)가 확인되었다(Fig. 3). 일부 기저세포의 심한 괴사로 인하여 기저막이 단열된 부위도 관찰되었다. 모낭을 둘러싸고 있는 중층편평상피세포들도 현저하게 증식되어 있었다. 병변이 확인된 표피층에 인접한 진피층과 혈관 주위로 미약한 내지 중등도의 중성호성백혈구 및 림프구가 침윤되어 있었다. 피부에 대한 Gram 염색 결과 손상된 일부 표피층과 가피 형성 부위를 중심으로 Gram 양성의 구균 집락이 확인되었다(Fig. 2, insert). 자돈의 피부 병변에 대한 PCR 결과, 두 개체 모두에서 524 bp의 SWPV 특이 밴드를 확인할 수 있었다(Fig. 4). 또한 피부 병변에서는 Staphylococcus hyicus가 순수 분리되었다. 검출된 PCR 양성밴드에 대한 염기서열분석 결과, SWPV의 VLTF-3 유전자 부위에 해당하는 염기서열을 확인하였고 NCBI의 GeneBank에 등록하였다(accession No. MT335811). 상기 염기서열에 대한 계통 분석 결과, 본 증례에서 검출된 SWPV는 미국, 브라질 및 인도에서 보고된 SWPV와 하나의 그룹을 이루면서 그 외 goatpox, sheeppox, monkeypox, vaccinia 및 fowlpox 바이러스와는 구분되어 있음을 확인하였다(Fig. 5). 따라서 본 증례는 육안 및 병리조직학적 소견과 미생물학적 검사 결과를 토대로 2차 세균 감염을 동반한 신생 자돈의 선천성 SWP로 최종 진단되었다.

Note multiple well-circumscribed, red to purple red raised, round papules, and pustules on the entire body of a neonatal piglet.

Severe epidermal hyperplasia with ballooning degeneration of stratum spinosum keratinocytes (hematoxylin and eosin; scale bar = 50 µm). Note the numerous Gram-positive cocci in the epidermal lesions (insert) (Gram stain; scale bar = 20 µm).
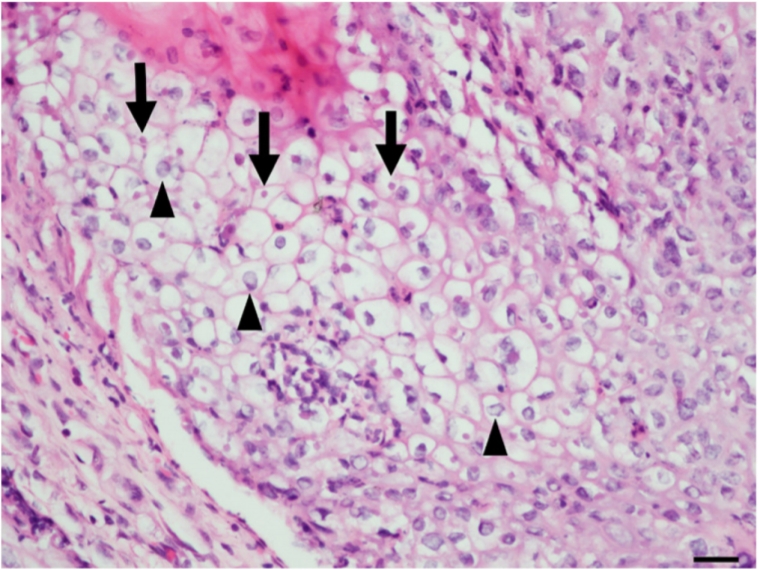
Note the eosinophilic intracytoplasmic inclusion bodies (arrows) and central nuclear vacuolation (arrowheads) in the degenerated keratinocytes (hematoxylin and eosin; scale bar = 20 µm).

Polymerase chain reaction products of swine poxvirus from the skin lesions in the piglets (lane M, 100 bp DNA ladder; lanes 1 and 2, skin tissues; lane 3, negative control).

Phylogenetic tree based on the amino acid sequence alignment of viral late transcription factor-3 genes in various poxviruses. The circle dot indicates the virus detected in this study.
SWP의 임상 진단은 피부에서 관찰되는 육안 병변에 기초한다. SWP의 병변은 주로 몸통 부분과 사지, 귀 등에서 호발하고 선천성 감염의 경우에는 두부를 포함한 전신에 걸쳐 병변이 관찰된다[8]. 감염 초기에는 편평하고 창백한 원형의 반점(macule)상 병변을 보이다가 시간이 경과하면서 홍반(erythema) 또는 표면으로부터 1-2 mm 가량 융기된 구진 형태로 변화한다. 이후 병변은 배꼽과 같은 모양으로 중심이 함몰되고 위축되며, 표면에 형성된 가피는 시간이 지나면서 탈락한다[4,8]. 본 증례에서는 출생하면서 전신의 피부 병변이 형성되어 있었고, 점차 구진성 병변과 더불어 국소 궤양과 가피 형성과 같은 진행형 병변의 특징을 나타내어 이미 모체 내에서 감염이 성립된 것으로 판단하였다. 선천성 SWP는 과거에도 보고된 바 있으나 일반적으로 흔하지 않은 편이다[2,4]. 국내에서는 1985년 경남 창원 소재 농장에서 2-3개월령 자돈에서 발생한 SWP 사례가 보고된 바 있다[7]. 해당 농장에서 SWP의 발생 원인은 불분명하나 출생 이후 불결한 사육 환경에서 이 질병을 매개하는 외부 기생충의 빈번한 노출에 의한 기계적 전파로 추정되었기 때문에 본 증례와는 차이가 있었다. 본 증례와 관련하여 발생 농장의 전반적인 위생 관리 상태, 감염성 질병 발생 상황 및 모돈의 번식 성적을 확인한 결과, 발생 전후 시점에서 두드러진 이상은 확인하지 못하였다. 또한 발병 이후, 전 모돈에서 분만된 신생 자돈 중에서 SWP에 이환된 개체는 추가로 나타나지 않았다. 국내 양돈 농장에서 SWP에 대한 진단 사례는 1985년 보고 이래 거의 전무한 실정으로 국내 SWP 발병 정도나 특징에 대해서는 아직 명확히 조사된 바가 없다. 따라서 SWP의 발생 원인을 규명하기 위해서는 보다 추가적인 조사가 필요할 것으로 사료된다. 본 증례를 통하여 국내 농장에서 여전히 SWPV가 자돈 피부병의 주요 원인 중 하나임을 입증할 수 있었으며, 임신 중인 모돈이 바이러스에 노출되었을 경우에는 자돈에 수직감염이 성립될 수 있음이 확인되었다. 아직까지 선천적인 SWP 감염의 병인은 확실히 밝혀져 있지 않다. 모돈에서 낮은 수준의 바이러스혈증 상태에서 태반감염에 의해 SWPV가 태아에 감염되는 것으로 추측되고 있다[4].
SWP에 대한 실험실적 진단은 병리조직학적 검사를 통하여 특징적인 표피층 세포의 변화를 관찰하고, 병변에서 SWPV를 검출함으로써 이루어진다[8]. 본 증례의 경우 병리 조직검사를 통하여 상피세포의 특징적 병변과 함께 세포질 내 바이러스 봉입체가 확인되었다. 그리고 PCR 기법을 이용하여 SWPV 양성 밴드를 검출하였으며, 증폭된 유전자의 염기서열 및 계통 분석에서 다른 지역의 SWPV와 동일한 그룹에 속하고 있음을 국내 최초로 규명함으로써 확진할 수 있었다. 분자생물학적 검사는 전자현미경 검사, 면역조직화학 염색 또는 바이러스 배양 등에 비해 간편하고 신속하게 진행할 수 있어 질병 진단에 널리 이용되고 있다. 돼지의 피부 질환 중 SWP와 감별해야 하는 대상으로는 수포성 질병, 피부 과민증, 화상, 물리적 창상, 연쇄상구균 및 포도상구균 등에 의한 세균성 피부염, 피부사상균증, 피부 옴 등의 외부기생충성 피부염이 있다[4,8]. 본 증례에서는 검사한 자돈 피부의 중층편평상피세포의 세포질에서 SWPV 특이 봉입체가 확인됨으로써 다른 감별진단 대상 질병을 용이하게 배제할 수 있었다.
일반적으로 SWP는 발병 후 한 달 이내에 자연적으로 회복될 수 있는 것으로 알려져 있지만, 2차 세균 감염이 동반되면 회복이 지연되기도 한다[8]. 본 증례에서는 병리조직검사상 피부 병변에서 그람 양성구균이 확인되었으며, 세균배양검사를 통하여 S. hyicus가 분리되었다. S. hyicus는 자돈에서는 삼출성 표피염의 원인체이지만, 건강한 성돈의 피부에서 상재하는 정상세균총으로 돈사 내 환경에도 흔하게 검출되는 것으로 알려져 있다[11]. 삼출성 표피염의 발병은 개체 간 싸움이나 돈사에서 유발되는 창상, 영양결핍, 환기불량, 다습한 환경 외에도 외부기생충, 피부사상균과 더불어 SWPV 같은 바이러스 감염 등 선행 인자에 의해 심화될 수 있다[11]. 본 신생 자돈의 경우 임신 중에 이미 SWPV 감염으로 인해 피부에 병변이 형성되어 출산한 직후 S. hyicus에 노출되었으며, 정상적인 피부에 비하여 방어 기제가 약화된 병변 부위에서 더욱 쉽게 균체가 증식하여 병증을 악화시켰을 것으로 판단되었다. 따라서 삼출성 표피염이 지속적으로 문제가 있는 농장의 경우, 환경적인 발병 요인 점검과 더불어 실험실 검사를 통하여 SWP 개재 여부를 확인하면 근본적인 발병 원인 파악에 도움이 될 것으로 사료된다.
SWP 발생은 농장의 불결한 위생 상태와 밀접한 관련이 있는 것으로 알려져 있다[8,9]. 최근 국내에서 양돈 시설 및 사양 기술의 발전으로 SWP 발생은 흔하지 않으나, 본 연구를 통하여 국내에서도 SWPV의 수직감염에 의한 선천성 발병이 있음을 확인할 수 있었다. 어린 자돈의 피부 질병은 만성적인 성장지연과 사료효율 감소로 인하여 농장에 큰 경제적 피해를 줄 수 있기 때문에, 자돈 피부에 이상 소견이 발생하였을 경우에는 반드시 실험실 검사를 의뢰하여 정확한 진단과 예방 대책 마련을 하는 것이 추천된다.
Notes
The authors declare no conflict of interest.
Acknowledgements
본 연구는 농림축산검역본부 학술연구용역과제(Z-1543083-2017-18-01) 연구비를 지원받아 수행되었으며, 이에 감사드립니다.
