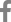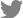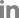|
 |
| Korean J Vet Res > Volume 61(4); 2021 > Article |
|
Abstract
Acknowledgments
Fig.┬Ā1.

Fig.┬Ā2.

Fig.┬Ā3.
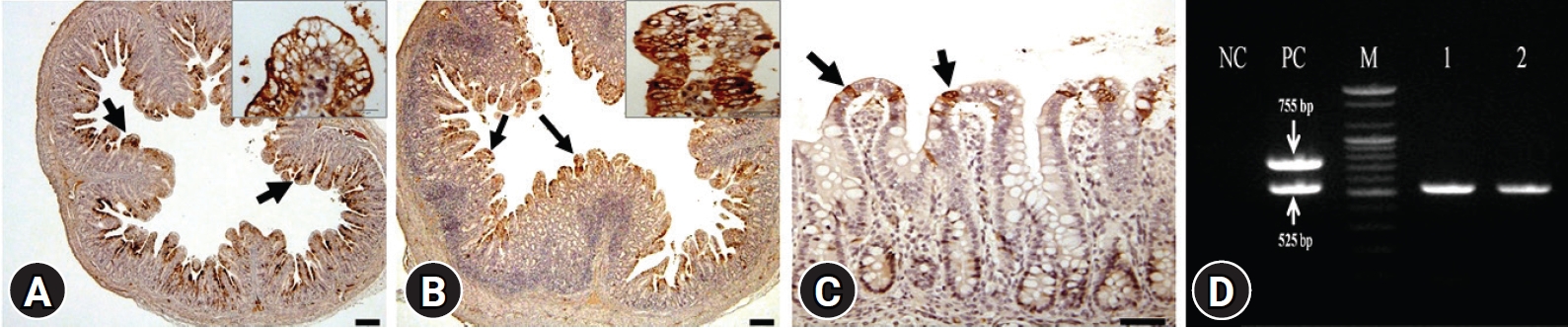
Fig.┬Ā4.
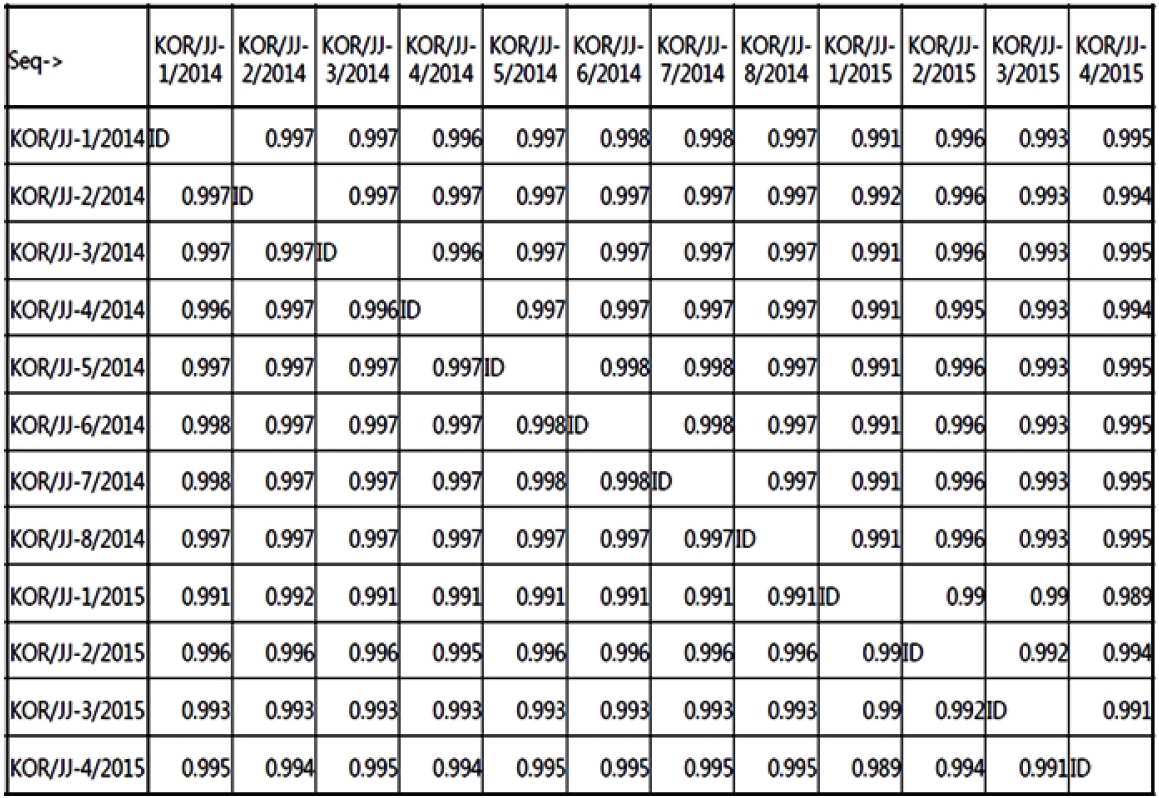
Fig.┬Ā5.
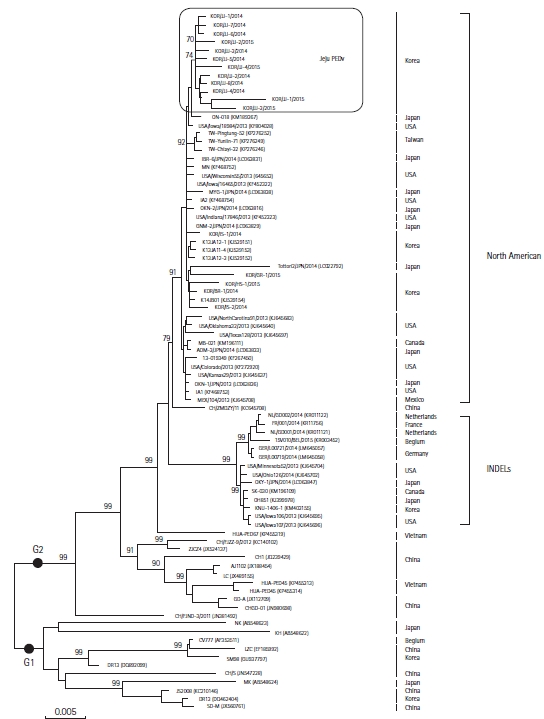
Table┬Ā1.
Table┬Ā2.
Table┬Ā3.
Table┬Ā4.
Table┬Ā5.
Table┬Ā6.
| Organ | Ages (d) |
Grade |
Average EG (mean ┬▒ SD) | ||||
|---|---|---|---|---|---|---|---|
| EG0 | EG1 | EG2 | EG3 | Total (%) | |||
| Jejunum | < 4 (n = 86)ŌĆĀ | 16 | 7 | 9 | 54 | 70 (81.4) | 2.17 ┬▒ 1.20* |
| 4-7 (n = 40)ŌĆĀ | 4 | 1 | 6 | 29 | 36 (90.0) | 2.50 ┬▒ 0.96* | |
| Ōēź 8 (n = 9) | 4 | 0 | 0 | 5 | 5 (55.6) | 1.67 ┬▒ 1.58* | |
| Total (n = 135) | 24 | 8 | 15 | 88 | 111 (82.2) | 2.24 ┬▒ 1.17 | |
| Ileum | < 4 (n = 80)ŌĆĀ | 12 | 3 | 9 | 56 | 68 (85.0) | 2.36 ┬▒ 1.11* |
| 4-7 (n = 38)ŌĆĀ | 3 | 3 | 2 | 30 | 35 (92.1) | 2.55 ┬▒ 0.95* | |
| Ōēź 8 (n = 9) | 3 | 1 | 0 | 5 | 6 (66.7) | 1.78 ┬▒ 1.48* | |
| Total (n = 127) | 18 | 7 | 11 | 91 | 109 (85.8) | 2.38 ┬▒ 1.10 | |
| ColonŌĆĪ | < 4 (n = 88) | 69 | 9 | 3 | 7 | 19 (21.6) | 0.41 ┬▒ 0.89 |
| 4-7 (n = 36) | 30 | 5 | 1 | 0 | 6 (16.7) | 0.19 ┬▒ 0.47 | |
| Ōēź 8 (n = 9) | 8 | 0 | 0 | 1 | 1 (11.1) | 0.33 ┬▒ 1.00 | |
| Total (n = 133) | 107 | 14 | 4 | 8 | 26 (19.5) | 0.35 ┬▒ 0.81* | |
References
- TOOLS
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 3,046 View
- 63 Download
- ORCID iDs
-
Hyeon-Ju Kim

https://orcid.org/0000-0003-0577-7938Hyoung-Seok Yang

https://orcid.org/0000-0003-4500-8826Sang Chul Kang

https://orcid.org/0000-0003-2845-981XJae-Hoon Kim

https://orcid.org/0000-0002-4410-9126 - Related articles
-
Prevalence and pathologic study of porcine salmonellosis in Jeju2017 December;57(4)
Reemergence of porcine epidemic diarrhea virus on Jeju Island2014 ;54(3)


 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print